A genomika, a genomalapú, genomléptékű biológia az emberiség intellektuális teljesítményeinek egyik legkiemelkedőbb sikere a 3. évezred kezdetén. A hatalmas és naponta bővülő, interneten elérhető adatbázisok, a high throughput technológiák (például génlapka vagy génchip) és az elképesztő ütemben fejlődő bioinformatikai eszközrendszer együtt új minőséget produkáltak az immunológiában is. Ez az immungenomika területe, melynek első világkongresszusát a Magyar Immunológiai Társaság rendezte 2004. október 3-7. között Budapesten. A kezdeményezés nem várt hatalmas sikere az eltelt hónapok alatt is világszerte ráirányította a figyelmet erre a területre (Wang - Falus, 2004).
Az egészséges és beteg szervezet immunológiai folyamatai (hasonlóan szinte minden életjelenséghez) annyira összetettek és annyira szerteágazóan és több szinten (sejten belül, sejtkapcsolatokban, szervek között, a szervezet és a populáció szintjén) reguláltak, hogy a kérdések valódi megközelítésére ma már kizárólag a systems biology kísérelhet meg választ adni. Ez a biológiát alapvetően átható rendszerszemlélet egyedi komponensek (molekula, sejt, szerv, szervezet) helyett azok hálózataiban gondolkodik, legyenek azok a génkifejeződést szabályozó molekulahálózatok vagy sejtek kapcsolatai. Minthogy ez a megközelítés a hálózatok elemeinek aktivitását szimultán vizsgálja, ezeket a jelenségeket csak a nagy teljesítőképességű kvantitatív genomikai technológiákkal lehet követni. Ennek megfelelően a könnyen hozzáférhető hatalmas adatmennyiség kiértékelése számítógépekkel történik, mert a jelenségek komplexitását csak informatikai algoritmusok képesek kezelni (Brusic - Petrovsky, 2003; Brusic, 2003, URL5).
Az immunológia kiemelkedő területe a "systems biology"-nak; több okból:
1. az antigénreceptorok repertoárjait kombinatorikus eseménysor (génátrendeződés és szomatikus hipermutáció) hozza létre
2. a molekuláris és celluláris kölcsönhatások jól vizsgálhatóak
3. komplex genetikai és jelátviteli utak tanulmányozhatóak
4. in vitro (például sejtkulturákban) és in vivo (például vakcináció követése) kísérletek egyaránt viszonylag könnyen megvalósíthatóak
5. nagyszámú adat keletkezik mérésenként
6. jó modellek (például immunológiai betegségek, transzgenikus állatok) állnak rendelkezésre
7. már ma is nagy betegség-adatbázisok (például MHC, vírusok, allergom) léteznek.
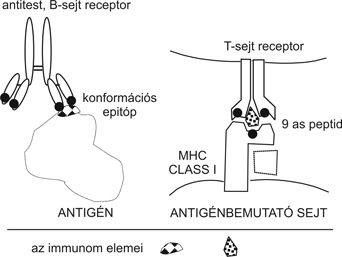
Az immunválasz során három univerzum találkozik (1. ábra), az egyedek örökölt genetikai tulajdonságai az MHC szintjén (= a populáció sokfélesége), az egyedek szerzett tulajdonságai az antigénreceptorok repertoárjaiban (= az egyeden belüli sokféleség) és az antigének összességének (immunome) heterogenitása (= a külvilág sokfélesége) (1. táblázat). Ehhez járul a "természetes immunitás" (pl. peptidtranszporterek - TAP, sejtadhéziós kapcsolatok, Toll receptorok, citokinek és receptoraik, komplementrendszer stb.) jelentős genetikai varianciája.
Ezek a számok óriási variációs és potenciális eseményhalmazt jelentenek az immunválasz során, melynek értékelését és analízisét kizárólag az informatika (immuninformatika) képes elvégezni.
Erre a kihívásra az immuninformatikával párosult genomikai alapon álló immunológia képes csak. A jövő immunológiája az immunomika, amely az immungenomika, az immunproteomika és az immuninformatika megfelelő szintézisét jelenti. Ez pedig nem más, mint a korszerű genomléptékű immunológia megfelelő kombinációja a számítástechnikával. (2. ábra). A genomikai analízis SNP (single nucleotide polymorphism-pontmutáció) és expressziós szintű megközelítést, proteomikai kutatást hatalmas, a peptidkönyvtárak monitorozását, és az MHC egyedi szerkezete alapján peptid-illesztő szoftverek sokaságát jelenti már ma is, és nyújtja még inkább a közeljövőben például a védőoltások kifejlesztésében (Brusic - August, 2004; Sette et al., 2005; Doytchinova et al., 2003; URL2; URL6; URL3). Hatalmas fejlődés várható az immunológiai epigenetikában is (például: glikoziláció).
Ez a fejlődés fog elvezetni az in silico megközelítésű prediktív, az egyed genetikai hátterét értékelő immundiagnosztikához, a személyre szabott immunterápiákhoz (például az "intelligens" antimikrobiális és antitumor vakcinák előállítása), a jelátviteli genomika, és ezzel együtt az immunfarmakogenomika új korszakához. Az eredményalapú virtuális immunrendszereket is igénybe vevő kutatás potenciális gyógyszertargetek sokaságát fogja felszínre hozni az autoimmun, fertőző, gyulladásos, allergiás (például biztató immunomikai távlatok látszanak az allergiás de-immunizáció területén (URL4; URL1; Sette et al., 2005), és egyéb klinikai kihívásokkal kapcsolatban is.
A jelen szám szerzői alapkutatási és klinikai immunológiai kérdések során egy szempontból hasonló következtetésre jutnak: az immunológia jövőjét a genomikával és a komputertudománnyal való találkozás alapvetően megváltoztatta.
Jövőre, 2006. október 8-12. között újra Magyarország látja vendégül a világ azon immunológusait, akik genomikai és informatikai érdéklődéssel foglalkoznak az immunválasz kérdéseivel.(2nd Basic and Clinical Immunogenomics és 3rd International Immunomics Congress).
Kulcsszavak: immunológia, genomika, immuninformatika, immunom, immunomika

1. ábra * A külvilágnak azon része (immunom) amely az immunrendszerrel reagál, kapcsolatba lép az antigénreceptorokkal (antitest a B-sejtek és T-sejt receptor a T-sejtek membránján). Ez az egyén szintjén megvalósuló polimorfizmus. Utóbbi esetében a populációs polimorfizmust reprezentáló MHC is szerepet kap az epitóp (9 aminosavas peptid) bemutatásában. A variábilis elemeket az antigénreceptorok (antitest, T-sejt receptor) és az MHC molekulán fekete körök jelzik. Az immunom a külvilág varianciáját reprezentálja.
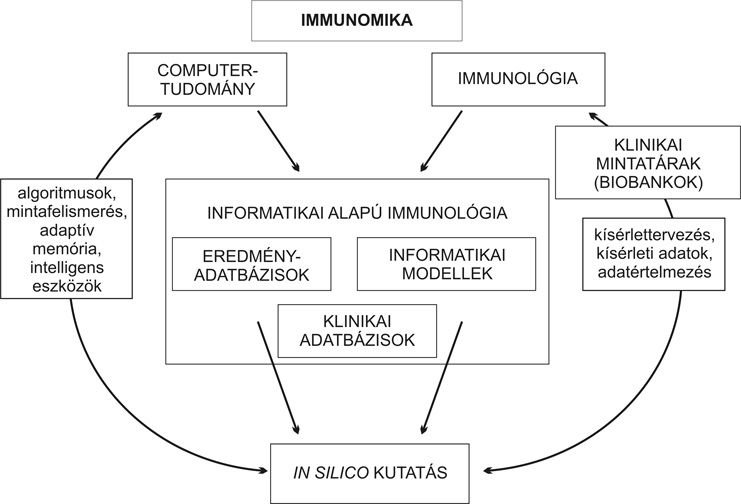
2. ábra * Az immunomikai szemlélet és kutatás folyamatábrája
Az immunválasz egyes elemei emberben Potenciális elemszám MHC I. osztályú haplotípusok 1013 T-sejt receptorok (TCR) 107-1018 B-sejt (antitest) klonotípusok 1012-1013 lineáris (kilenc aminosavból álló) TCR peptid epitóp 1011 konformációs epitóp 10111. táblázat
Irodalom
Brusic, Vladimir (2003): From Immunoinformatics to Immunomics. Journal of Bioinformatics and Computational Biology. 1, 179-81.
Brusic, Vladimir - August, J. Thomas (2004): The Changing Field of Vaccine Development in the Genomics Era. Pharmacogenomics. 5, 597-600.
Brusic, Vladimir - Petrovsky, Nikolai (2003): Immunoinformatics - The New Kid in Town. Novartis Foundation Symposium. 254, 3-13.
Doytchinova, Irini A. - Taylor, P. - Flower, D. R. (2003): Proteomics in Vaccinology and Immunobiology: An Informatics Perspective of the Immunone. Journal of Biomedicine and Biotechnology. 5, 267-290.
Sette, Alessandro - Fleri, W. - Peters, B. - Sathiamurthy, M. - Bui, H. H. - Wilson, S. A. (2005): Roadmap for the Immunomics of Category A-C Pathogens. Immunity. 22, 155-61.
Wang, Ena - Falus András (2004): Changing Paradigm through a Genome-based Approach to Clinical and Basic Immunology. Journal of Translational Medicine. 2, 2-3.
URL1: http://fermi.utmb.edu/SDAP/
URL2: http://research.i2r.a-star.edu.sg/multipred/
URL3: http://wehih.wehi.edu.au/mhcpep/
URL4: http://www.allergome.org/
URL5: http://www.immunomicsonline.com/
URL6: http://www.syfpeithi.de/