AZ öregedésről – A hálózatok szemszögéből
|
|
Csermely Péter |
Sőti Csaba |
|
|
|
az MTA doktora, Semmelweis Egyetem |
PhD, Semmelweis Egyetem Orvosi Vegytani, |
|
|
|
Orvosi Vegytani, Molekuláris Biológiai |
Vegytani, Molekuláris Biológiai |
|
|
|
és Pathobiokémiai Intézet |
és Pathobiokémiai Intézet |
|
|
|
csermely @ puskin.sote.hu |
csaba @ puskin.sote.hu |
|
A biológiának kevés olyan komplex jelensége van, mint az öregedés. Annak ellenére, hogy az utóbbi években egyre több „öregedés-gént” sikerült megtalálni, az öregedés molekuláris magyarázatára szolgáló elméletek szinte mindegyike rendszerszemléletet alkalmaz, és a hálózatos megközelítéssel jól összhangba hozható. Cikkünkben e gondolatmenetet követve foglaljuk össze az öregedő hálózatok, öregedő sejtek és szervezetek legfontosabb sajátosságait. Az öregedésre jellemző véletlen hibák a hálózatok gyenge kölcsönhatásainak károsításával és moduljaik szétkapcsolásával hozzájárulnak az öregedő rendszerek növekedő instabilitásához, dezintegrálódásához és zajához. A csökkenő energiaforrások miatt az öregedő rendszer a legfontosabb funkciókra korlátozza magát. Mindezen folyamatokat a fiatal rendszerekben észrevétlen maradó, de a megnövekedett zaj miatt az öreg rendszer ingerküszöbén „átcsúszó” jelekre adott válaszok egy hálózati szinttel feljebb is hangsúlyossá teszik. A jelenleg egyre jobban elterjedő multi-target gyógyszerek és gyógyszerkombinációk hatékonyan segíthetik az öregedő szervezetet e káros hatások kivédésében.
Sejtes hálózatok
A sejtben kétfajta hálózatot szoktunk megkülönböztetni. A felépítés szempontjából beszélhetünk fehérje-fehérje kölcsönhatási hálózatról, továbbá a sejt szerkezetét fenntartó és a sejtet mozgató citoszkeleton hálózatáról és a sejtszervecskék (például mitokondriumok) membránokkal összekötött hálózatáról. Ezek mind fizikai struktúrákat jelölnek. A fehérje–fehérje kölcsönhatási hálózatok két fehérje fizikai kölcsönhatásának sok-sok sejten értelmezett valószínűségét adják meg. Ezzel szemben a citoszkeleton és a sejtszervecskék hálózatai konkrét kölcsönhatásokat jelölnek, amelyek létrejöttéhez számos fehérje-fehérje kölcsönhatás is szükséges. Funkcionálisan beszélhetünk a sejtbeli metabolikus hálózatokról, jelátviteli hálózatokról és génexpressziós hálózatokról, amelyekben a kölcsönhatások sok esetben nem direkt, fizikai kölcsönhatások, és így e hálózatok gráfokként interpretálhatóak. A metabolikus hálózatokban a hálózat elemei a sejt kisméretű kémiai molekulái (például szőlőcukor, adenin stb.) és a kölcsönhatások a molekulákat egymásba alakító reakciók, amelyeket enzimek katalizálnak. A sejt jelátviteli mechanizmusai is hálózatot alkotnak, amely átfed a gének kifejeződését szabályozó gén-expressziós hálózattal (Sőti et al., 2005).
A hálózatok egyik legfontosabb feladata a rendszer alkotóelemei közötti kommunikáció biztosítása. Az élő rendszerek mindegyike nyitott, így hálózataik határait bizonyos értelemben mesterségesen jelöljük ki, hiszen azok a „környezettel” is kapcsolatban állnak. A hálózaton belüli kommunikációnak három fontos feladata van.
(1) A hálózatot kívülről érő vagy a benne keletkező zavar, zaj hatékony „eltüntetése”, disszipációja. Ezt a hálózatok moduláris felépítése és a skálafüggetlen fokszámeloszlásából adódó csomópontjai segítik.
(2) A hálózatot érő jelek hatékony továbbítása. Ezt a hálózatok távoli pontjait összekötő, többnyire gyenge kapcsolatai segítik, amelyek a hálózatokat kisvilággá teszik.
(3) A zajok és jelek megkülönböztetése. Ez a hálózat „tanulóképességét” igényli, amellyel a közel azonos formában visszatérő, nagyobb intenzitású zajokra szerkezetének megfelelő átalakításával speciális választ fejleszt ki (Csermely, 2006). A hálózatok tanulóképességéhez (bizonyos nagyvonalúsággal: evolúcióképességéhez, evolvabilitásához) szükséges topológiai sajátosságok még nem kellőképpen ismertek. Az öregedő hálózatokban mindhárom fenti funkció sérül, illetve részben összekeveredik. Ennek eddig ismert mechanizmusait, illetve a védekezés eddig megismert módjait foglaljuk össze a továbbiakban.
Az öregedés hálózatos okai
Az öregedő sejtek és szervezetek zaja folyamatosan nő. E rendszerekben a zaj olyan kismértékű és véletlenszerű változásokat jelöl, amelyek nem a rendszerek szokásos, begyakorolt és a legtöbb esetben igen nagy erősítéssel járó válaszai, hanem akár a sejtek egyik vagy másik folyamatából származó belső zajok, akár pedig azok a kismértékű külső változások, amelyekre az érkező jelekkel ellentétben a sejtnek nincs begyakorolt válasza, és amelyeket az öregedő sejt nem tud gyorsan és hatékonyan eltüntetni, disszipálni. Az öregedő sejt zajának növekedésével párhuzamosan a rendszerek integritása és komplexitása csökkenésnek indul. Ráadásul e két folyamat kölcsönösen erősíti egymást. A megnövekedett zaj olyan alacsony jeleket is átmenetileg az ingerküszöb fölé emel, amelyek egy fiatal szervezet alacsony zaja mellett soha nem kerülnének az ingerküszöb fölé, s így észrevétlenek maradnának. E folyamatot véletlenszerű ingerküszöb-átlépésnek nevezhetjük (ez a kifejezés az angolszász irodalomban használt stochastic resonance átírása oly módon, hogy a magyar változat ne tartalmazza a fizikusoknál más fogalomkörre használt rezonancia szót; 1. ábra). A jelenség az öregedő szervezet fokozódó mértékben véletlenszerű válaszainak egyik oka lehet (Sőti – Csermely, 2006).
Az öregedés egyik legfontosabb oka a rendszer véletlenszerű kopása, amelyet a sejtekben legnagyobbrészt a szabad gyökök károsító hatása okoz. Ennek egyik érdekes következménye, hogy a földön élő emlősállatok átlagosan hárommilliárd szívdobbanás után meghalnak, függetlenül attól, hogy patkányok-e, amik esetén ez négy év alatt következik be, vagy emberek, akiknél ehhez mintegy száz-százhúsz év szükséges. Ennek a hátterében az áll, hogy a patkány mitokondriumai időegység alatt negyvenszer annyi szabad gyököt produkálnak, mint az emberi mitokondriumok. Érdemes itt arra is utalni, hogy az öregedés visszafogásának eddigi egyetlen általános lehetősége a kalóriamegvonás. Ebből következően, aki kevesebb esélyt ad a mitokondriumainak a szabad gyök produkálására a túlzott kalóriabevitel elkerülésével, az akár tíz évvel is meghosszabbíthatja a várható élettartamát (Csermely, 2005).
Az öregedő hálózatok, azaz cikkünk szempontjából azok a hálózatok, amelyekben folyamatosan számottevő mennyiségű véletlen hiba generálódik, fokozatosan elveszítik a globális jeltovábbítás képességét (Chan et al., 2004). A hálózatok „távoli”, globális kapcsolatai általában gyengék. E gyenge kapcsolatok mértéke az öregedő hálózatokban legalább három ok miatt csökken:
(1) A hálózatok véletlenszerű károsodása elsősorban a nagy többségben jelen lévő gyenge kapcsolataikat szünteti meg.
(2) A gyenge kapcsolatok számát az is csökkenti, hogy az öregedő sejt energiatermelése sérül, s a csökkenő mértékű energiát a hálózat a legfontosabb, erős kapcsolatainak fenntartására használja, akár korábbi elrendezésének teljes átalakításával, ún. topológiai fázisátmenettel. Ezen átalakulás során az öregedő hálózat a működését egyre inkább a hálózat vázára (szkeletonjára) vonja vissza.
(3) A sejt fehérjéi közötti gyenge kapcsolatok azáltal is sérülnek, hogy a sejtben felgyűlnek a kijavíthatatlanul sérült fehérjék, amelyek aggregálni kezdenek. Ezek az aggregátumok magukhoz vonzzák a gyenge kapcsolatokban lévő sejtes fehérjék egy részét is (2. ábra).
A gyenge kapcsolatoknak a fenti három ok miatt bekövetkező relatív hiánya az öregedő hálózatban hozzájárul a hálózat fokozott zajához, integritásának és komplexitásának csökkenéséhez (Csermely, 2005, 2006; Derényi et al., 2004; Promislow, 2004; Sőti – Csermely, 2006).
A fenti értelemben vett „öregedő hálózatok” csoportstruktúrája, moduláris szerkezete is fokozatosan dezintegrálódni kezd. Ez egyrészt a modulokat összekötő gyenge kapcsolatok sérülésére vezethető vissza, de a sejtekben szerepet játszik a bennük lévő modulokat (például fehérjekomplexeket vagy mitokondriumokat) összekötő, dajkafehérjék által biztosított kapcsolatok speciális sérülékenysége is. E sérülékenység a dajkafehérjék integráló hatásaival függ össze, és arra vezethető vissza, hogy a károsodott fehérjéknek az öregedő sejtet elöntő tömege kompetitíven kiszorítja a dajkafehérjékkel alkotott komplexekből az eredetileg ott lévő és a sejt moduljainak összekapcsolását biztosító fehérjepartnereket. Ez a jelenség azonban már átvezet az öregedő hálózatok védelmi mechanizmusaihoz, hiszen a modulok szétkapcsolása megakadályozza a károsodás átterjedését az egyik modulról a másikra (Sőti – Csermely, 2006).
Öregedő hálózatok javításának módjai
A csomópontok kiemelkedő szerepét már régebben feltárták az öregedő hálózatok működőképességének fenntartásában (és – valószínűleg – a hálózat zajának csökkentésében). Az öregedő hálózatokban túlterhelődő csomópontok alternatív útvonalakkal tehermentesíthetők. A csomópontok tehermentesítésében – paradox módon – a hálózat karcsúsítása is segíthet, azaz akkor, amikor az öregedő sejt az előzőekben leírt módon a legfontosabb útvonalaira korlátozza magát, nemcsak energiát spórol, hanem a csomópontjait is védi a túlterhelés ellen (Promislow, 2004; Ferrarini et al., 2005; Motter, 2004).
A hálózatok gyenge kapcsolatait olyan beavatkozások is erősíthetik, amelyek több helyen hatnak, és az egyes elemek működését csak részben befolyásolják. Az ilyen multi-target gyógymódra alkalmas gyógyszerek vagy gyógyszer-kombinációk kifejlesztése jelenleg egyre nagyobb teret kap. E gyógyszerek az adott betegségre gyakorolt hatásuk, kisebb dózisukból fakadó kisebb toxicitásuk, mellékhatásaik és rezisztenciát okozó hatásaik mellett a beteg szervezet sejtjeit valószínűleg még stabilizálhatják is, és ilyen módon is hozzájárulhatnak az egészséges, zajmentesebb állapot visszaállításához. Ezek a gyógymódok a különböző kemoterapeutikumok kombinációja révén egyre nagyobb teret kapnak a rák gyógyításában, de használatosak a baktériumok rezisztenciájának leküzdésében vagy az AIDS gyógyításában is. Az egyszerre több támadásponton, de kis affinitással, gyenge kölcsönhatással ható, multi-target gyógyszerek igen nagy szerepet kaptak a pszichés megbetegedések, illetve a cukorbetegség gyógyításában (Csermely et al., 2005).
Kulcsszavak: gyógyszerkombinációk, hálózatok, hálózati modulok, ingerküszöb, öregedés
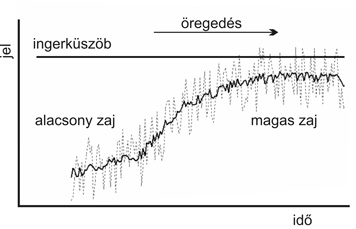
1. ábra • Az öregedő hálózatok egyre fokozódó véletlenszerű viselkedésének egyik lehetséges oka: a véletlenszerű ingerküszöb-átlépés. Az öregedő hálózatok megnövekedett zaja olyan jeleket is az ingerküszöb fölé emel, amelyek egy fiatal hálózat mérsékelt zaja esetén észrevétlenek maradnának. Mivel a zaj a különböző pillanatokban és a különböző sejtekben, szervezetekben más és más, az esély, hogy a rendszer véletlenszerű ingerküszöb-átlépéssel válaszol a hatásokra, elég kiszámíthatatlan, ami fokozza az öregedő hálózatok válaszainak esetlegességét.
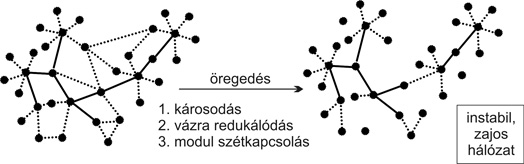
2. ábra • Az öregedő hálózatok átrendeződései. Az öregedő hálózatokat érő folyamatos, véletlenszerű károsodás, a hálózat erőforrásainak a csökkenése és védelmi mechanizmusainak beindulása szétkapcsolja a hálózat moduljait, csökkenti a gyenge kapcsolatait és a hálózatot egyre jobban az erős kölcsönhatásaiból felépülő vázára redukálja. Ez a hálózat stabilitásának csökkenéséhez és zajának növekedéséhez vezet.
Irodalom
Chan, K. P. – Zheng, D. – Hui, P. M. (2004): Effects of Aging and Links Removal on Epidemic Dynamics in Scale-Free Networks. International Journal of Modern Physics B 18, 2534–2539.
Csermely Péter (2005): A rejtett hálózatok ereje. Vince, Budapest
Csermely Péter (2006): Weak Links: Stabilizers of Complex Systems from Proteins to Social Networks. Springer Verlag, Heidelberg
Csermely Péter – Ágoston V. – Pongor S. (2005): The Efficiency of Multi-Target Drugs: The Network Approach Might Help Drug Design. Trends In Pharmacological Sciences. 26, 178–182.
Derenyi Imre – Farkas I. – Palla G. – Vicsek T. (2004): Topological Phase Transitions of Random Networks. Physica A. 334, 583–590.
Ferrarini, Luca – Bertelli, L. – Feala, J. – McCulloch, A. D. – Paternostro, G. (2005): A More Efficient Search Strategy for Aging Genes Based on Connectivity. Bioinformatics. 21, 338–348.
Motter, A. E. (2004): Cascade Control and Defense in Complex Networks. Physical Review Letters. 93, 098701.
Promislow, Daniel E. (2004): Protein Networks, Pleiotropy and the Evolution of Senescence. Proceedings. Biological sciences. 271, 1225–1234.
Sőti Csaba – Csermely Péter (2006): Aging Cellular Networks: Chaperones As Major Participants. Experimental Gerontology. 41, In Press (www.Arxiv. Org/Q-Bio.MN/0605030).
Sőti Cs. – Pál Cs. – Papp B. – Csermely P. (2005): Cha-perones As Regulatory Elements of Cellular Networks. Current Opinion in Cell Biology. 17, 210–215.
<-- Vissza a 2006/11 szám tartalomjegyzékére
<-- Vissza a Magyar Tudomány honlapra
[Információk] [Tartalom] [Akaprint Kft.]