|
Ebből adódik a zeolitok szelektív adszorpciós
képessége, az ún. molekulaszűrés, ugyanis az a molekula, amelyik befér
az adott zeolit pórusába, ott adszorbeálódik, amelyik nem, az pedig
áthalad az adszorbens szemcsék között az oszlopon.
A molekulák mérete alapján egy adott elválasztási
feladathoz kiválasztható a megfelelő zeolit. Például a kálium-A
zeolit, (3A molekulaszűrő) segítségével szinte minden gáz
vízteleníthető, szárítható, mert molekuláik nem férnek be a zeolit
pórusaiba, így csak a víz kötődik meg. Különböző, zeolittartalmú
patronokat használnak a hűtőszekrények hűtőfolyadékának, a járművek
fékrendszerének, légkondicionáló berendezések zárt cirkulációs körében
és transzformátorolajoknál az esetleg bekerülő víz megkötésére.
Zeolitokat használnak szárító anyagként dupla falú ablakoknál is, ahol
a két légmentesen összeragasztott üveg közé különböző gázokat, például
argont tesznek a hő- és hangszigetelés javítására. A növekvő
energiaárak mellett az ablakok hőszigetelése egyre fontosabb, így az
itt használt zeolitok iránti igény is nő.
Nagyobb léptékű szárításnál, például hidrogén- vagy
oxigéngázáramok esetében golyókká vagy kis hengerekké formázott
zeolitot használnak. Ezek a dinamikus műveletek folyamatos
regenerálást is feltételeznek. Az 5. ábrán két jellegzetes
adszorpciós izoterma látható, amelyeken az egyensúlyi nyomás
függvényében az adszorbens tömegegysége által megkötött
anyagmennyiséget tüntettük fel. Látszik, hogy az
adszorpciós-deszorpciós ciklus végbemenetelének egyik lehetősége az,
hogy alacsonyabb T2 hőmérsékleten történik az adszorpció,
míg magasabb T1 hőmérsékleten a deszorpció. A másik
lehetőség azonos hőmérsékleten, de különböző nyomáson végezni az ad-,
illetve deszorpciót. A fűtő-hűtő ciklus neve hőmérsékletváltó (thermal
swing), míg a nyomás csökkentésével regenerálóé nyomásváltó (pressure
swing) eljárás.
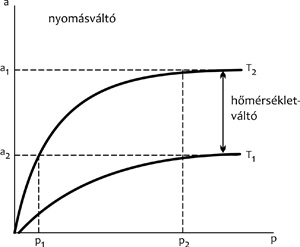
5. ábra • Adszorpciós izotermák
a regenerálási lehetőségek bemutatásával
Van egy harmadik lehetőség is: inert leszorító gáz
alkalmazása. Ezt a módszert általában a hőmérsékletváltó eljárással
kombinálva alkalmazzák.
Mind a 3A, mind a 4A zeolitot világszerte
használják csepfolyósított propán, halogénezett szénhidrogének és
földgáz szárítására. A 3A alkalmasabb olefineket (etilén, propilén)
tartalmazó krakkgázok és más olajfinomítói gázáramok szárítására, mint
a 4A, mert utóbbi pórusaiba ezek a kis szénatomszámú olefinek beférnek
és megkötődnek. A 4A nagyobb szénatomszámú szénhidrogének, benzol,
alkoholok szárítására használatos, és akkor, ha a vízzel együtt
szén-dioxidot is el kell távolítani, például a földgázból.
Legismertebb a földgáz tisztítása 4A zeolittal,
amely magában foglalja a H2S eltávolítását is. Ez nagyon
fontos környezetvédelmi szempontból. Amikor a megszokottnál nagyobb
kén- vagy nitrogéntartalmú molekulát kell adszorpcióval eltávolítani,
akkor a nagyobb pórusméretű 13X zeolitot használják.
A szárítás mellett a kén-dioxid és a nitrogén-oxidok megkötésére a
magyar természetes zeolitok, a mordenit és klinoptilolit is alkalmas.
Zeolitokkal megvalósítható klasszikus feladat a normál és
izoparaffinok szétválasztása. Bizonyos célokra, például benzinek
oktánszámának javítására az elágazó, más célokra, pl.
mosószergyártásra az egyenes láncú szénhidrogének a kívánatosak, ezek
könnyebben elbonthatók (miután évszázadokon át az állati zsíradékok
lúgos hidrolízisével főzött szappanokban lévő palmitin- és sztearinsav
fogyasztásához szoktak hozzá a természetes vizekben található
mikroorganizmusok.)
A hosszabb normál szénhidrogének kinetikus átmérője
a propánéhoz (0,43 nm) hasonló, míg a legegyszerűbb elágazó
szénhidrogén, az izobután is jelentősen nagyobb méretű (0,50 nm). A
CaA zeolit pórusmérete a kettő közé esik, így elválasztásukra kitűnően
felhasználható.
A kerozinból mosószeripari célokra a normál
szénhidrogéneket 350 oC-on kinyerő eljárás első, adszorpciós lépésében
a normál paraffinok megkötődnek, míg az elágazóak, mivel nem férnek be
a zeolit pórusaiba, áthaladnak az oszlopon. A 2. periódusban a nyomást
csökkentve a szemcsék közötti térből is távoznak az izoparaffinok, míg
a 3. periódusban leszorító gázok (NH3, H2)
alkalmazásával érik el a normál paraffinok deszorpcióját.
Egy másik nagyléptékű művelet a levegő
szétválasztása alkotórészeire (oxigén, nitrogén, nemesgázok). Ez
zeolitokkal általában alacsony hőmérsékleten történik, de egyre nő a
szobahőmérséklet körül működő, nyomásváltó berendezések száma is ipari
célú oxigén és nitrogén előállítására. Angliában A és X zeolitot
használnak oxigén előállítására kórházi, egészségügyi célokra.
Katalizátorok
A zeolitok első katalitikus alkalmazására 1959-ben került sor, amikor
a Union Carbide Co. kutatói izomerizációs reakciókban tesztelték az Y
zeolitot. 1960-ban javasolták az alakszelektív katalízis elnevezést
annak a váratlan katalitikus aktivitásnak a megjelölésére, amelyet
kalciumion-cserélt A zeolit (5A) esetében tapasztaltak. A 4–5 Å
pórusátmérőjű zeoliton szelektíven krakkolódtak az egyenes szénláncú
n-paraffinok, ugyancsak egyenes láncú termékeket adva.
Az X zeolit krakk katalizátorként való
alkalmazására 1962-ben került először sor, amikor kis mennyiségű
zeolitot téve a klasszikus amorf alumínium-szilikáthoz azt
tapasztalták, hogy jelentősen nőtt a katalitikus aktivitás.
A hatvanas évek végén és a hetvenes években
jelentős előrelépést jelentett a zeolitok szintézise területén új,
nagy szilíciumtartalmú, közepes pórusméretű anyagok (főleg a Mobil cég
ZSM sorozata) előállítása. Ezek az anyagok addig nem ismert,
alakszelektív átalakulásokra kifejlesztett technológiák
megvalósításához vezettek.
Ezzel párhuzamosan a zeolitok módosításában is
történt előrehaladás. Fémek és fém-oxidok beépítésével, új
dealuminálási technikák kidolgozásával, ioncserével mint a szintézist
követő legfontosabb módosításokkal sikerült jelentősen befolyásolni a
zeolitok aktivitását és szelektivitását.
Az 1980-as években kifejlesztett új
szintézismódszerekkel sikerült a Si és az Al helyettesítése más
elemekkel a zeolitrácsban. Ez és a szerkezetvizsgáló módszerek
fejlődése lehetővé tette számos új szerkezetű és összetételű zeolit
felfedezését és a konkrét alkalmazásoknak jobban megfelelő anyagok
előállítását.
Végül, a katalitikusan aktív helyek kialakítási
technikájának fejlődése révén, például fémek bevitelével és a
fémkomplexeknek a zeolitok csatornáiban, üregeiben való létrehozásával
a kémiai tulajdonságok olyan finoman változtathatók, hogy reálissá
vált a lehetőség az enzimkatalízis utánzására.
Zeolitok mint alakszelektív katalizátorok •
Amint már szerepelt, a zeolitok egyedi jellegzetessége az, hogy
egységes méretűek a pórusaik. A jelenleg rendelkezésre álló zeolitok
pórusainak mérete 4–13 Å közötti, ami megegyezik a petrolkémiában
fontos szénhidrogének méretével. Ilyen esetben nagyon kis változás a
molekula méretében nagyon megváltoztathatja a diffúzió jellemzőit.
Például az orto-xilol diffúziója ZSM-5 zeolitban három nagyságrenddel
lassúbb, mint a para-xilolé.
Reaktáns- és termékszelektivitás • A
jelenséget meghatározó paraméterek a molekulák és a zeolitcsatornák
mérete. Ha a betáplált anyagban különböző molekulák vannak, csak a
zeolit pórusainál kisebb méretű és megfelelő alakú molekulák képesek
bejutni a pórusokba, és ott reakcióba lépni. Ez a
reaktánsszelektivitás.
A másik eset az, amikor a reakciónak több terméke
is van, de csak azt érzékeljük, tudjuk detektálni, amelyik ki tud
diffundálni a zeolitkristályból. Ezért a termékösszetételt
nagymértékben befolyásolja a zeolit pórusainak és a termékmolekuláknak
a mérete. Ez a termékszelektivitás.
Átmenetiállapot-szelektivitás • Vannak
esetek, amikor a reaktáns és a termékmolekulák is képesek be- és
kidiffundálni a zeolit kristályokba(-ból). Ilyen esetekben is
megfigyelhető valamiféle szelektivitás. Ha egy bizonyos molekula olyan
átmeneti állapoton keresztül keletkezik, amelynek kialakulásához nincs
elegendő tér a zeolitcsatornában, a katalitikus centrum közelében,
akkor ezt a molekulát nem találjuk meg a termékek között. Ezt a
jelenséget átmenetiállapot-szelektivitásnak nevezik.
Zeolitok mint enzimszerű katalizátorok • az
enzimekhez hasonlóan a zeolitok tulajdonságai is nagyon egyediek,
amelyek a hatásos katalitikus működés alapját jelentik. Mindkét
katalizátortípus esetében a következő lépések a meghatározók:
• a reaktáns(ok) és a szubsztrát összekapcsolódása
nem kémiai kölcsönhatás révén,
• ezen kölcsönhatás jellegének befolyása a kémiai
reakcióra, beleértve a meglévő kémiai kötések felhasadását és újak
kialakulását, olyan átmeneti állapot(ok)on keresztül, amelyek
természetét a szubsztrát tulajdonságai határozzák meg.
A reaktáns kölcsönhatását a zeolittal (szubsztrát)
az előzőekben leírt alakszelektív hatások szabályozzák. Ráadásul a
zeolitrács üregei és csatornái mikroreaktorként, illetve az előre
eltervezett szimmetriájú, katalitikusan aktív helyek hordozóiként is
szerepelnek.
A reaktáns(ok) és a szubsztrát (enzim)
összekapcsolódása egy szupermolekulává emlékeztet a zeolitokban
kialakuló átmeneti állapot konfigurációjára. A zeolit a kívánt,
reaktáns- vagy termékszelektivitásnak megfelelő átmeneti állapot
stabilizálásával csökkenti a reakció aktiválási energiáját.
Ipari folyamatok zeolit alapú katalizátorokkal
Katalitikus krakkolás • Ez volt az első ipari eljárás, amelyben
zeolitokat katalizátorként alkalmaztak, és az elkövetkező években is
még ez marad a zeolit katalizátorok fő hasznosítási területe. Jelenleg
a kevéssé értékes nyersolaj frakciók krakkolása, a nagyobb
szénhidrogének C1–C6 molekulákká alakítása az egyik legfontosabb
gazolinforrás. Napjainkban a katalitikus krakkolást fluidágyas
technológiával végzik.
Ebben az előmelegített nyersolaj a regenerált
katalizátorporral találkozik, és együtt kerülnek a 450–500 oC
hőmérsékletű reakciózónába. Rövid érintkezés után (néhány másodperces
kontaktidő) a használt katalizátort és a termékeket egy következő
zónában elválasztják egymástól. Itt gőzöléssel távolítják el a
katalizátor felületéről az adszorbeált szénhidrogéneket, majd a
regenerátorban 600–800 oC-on levegővel leégetik az erősebben kötődött
ún. szénlerakódást. Ezután a regenerált katalizátort újra
visszavezetik krakkolásra. A szeparátorban kapott
termékszénhidrogéneket különböző frakciókra választják szét:
C1–C3-gázok, C4, gazolin, krakkbenzin, könnyűolaj, nehézolaj és
recirkulációs olaj. A nehezebb frakciókat visszavezetik krakkolásra.
Az előzőekben leírt folyamatot a 6. ábra mutatja (Venuto – Habib,
1979).
A jelenleg használatos katalizátor a faujazit
(zeolit) komponens (HY, ultrastabil Y, ritkaföldfém Y) és a
mátrixanyag keveréke. A különböző komponensek jól beállított arányával
lehet megfelelő termikus/hidrotermális stabilitást, mérgeződéssel
szembeni ellenállást (például fém Ni- vagy V-adalékkal), a zeolit és a
mátrix mennyiségének kiegyensúlyozásával pedig megfelelő mechanikai
tulajdonságokat (jó fluidizáló képesség, kopásállóság, kismértékű
porlódás) elérni. Hazánkban Százhalombattán működik ilyen technológia.
Zeolit katalizátorok a finomvegyszerek
gyártásában • Bár a zeolitok katalizátorként és
katalizátorhordozóként való hasznosításának fő területe a petrolkémia
marad, egyre több területen alkalmaznak zeolitokat az intermedierek és
finomvegyszerek gyártásában is. A homogén katalizátorok heterogénekkel
való helyettesítésének igénye iniciálta a kutatás fejlődését ezen a
területen. A fő alkalmazási terület a proton, illetve Lewis-sav
katalizálta reakciók, mivel a savas zeolitok alakszelektív
tulajdonságuk miatt előnyösen használhatók. Természetesen más funkciók
is beépíthetők a zeolitokba, és a sav-bázis tulajdonságok is
módosíthatók a szintézis során, például a Si és Al mellett más elemek
beépítésével a zeolitrácsba, vagy a szintézis után alkalmazott
dealuminálás, ioncsere, impregnálás révén. Ily módon a kívánt irányba
alakíthatók a zeolit katalizátorok tulajdonságai vagy kombinálhatók
más katalitikusan aktív centrumokkal a legjobb aktivitás és
szelektivitás elérése érdekében.
A zeolit katalizátorokkal végrehajtható reakciók a
kettős kötés izomerizáció, vázizomerizáció, dehidratálás,
dehidrogénezés, szubsztitúció aromás gyűrűben (halogénezés, acilezés,
alkilezés), aromások izomerizációja, szelektív hidrogénezés, szelektív
oxidáció.
Zeolitok a környezetvédelmi katalízisben • A
zeolitalapú katalizátorok a petrolkémiai eljárások kulcsfontosságú
anyagai. Jelenleg azonban az olajipar újabb kihívások előtt áll.
Ilyenek a légszennyezés csökkentése vagy a nehezebb olajpárlatok
minőségi javítása. A légszennyezés csökkentése a kipufogógázok, ipari
véggázok SOx- és NOx-tartalmának csökkentését
jelenti.
Aromatizálással nagy oktánszámú elegyek kaphatók
például C3–C4 frakciókból, vagy gyenge minőségű benzinekből. Azonban
az új szabályok a C4-tartalom (az erős párolgás elkerülésére) és a
benzoltartalom csökkentését írják elő. Különböző új eljárásokat
fejlesztettek ki az előírásoknak megfelelő benzinek előállítására.
Ezek egyenes szénláncú olefinek izomerizálása izoolefinekké, amelyek
metanollal éterezhetők, C3–C4 olefinek oligomerizációja, vagy benzol
alkilezése alkil-aromásokká. A n-paraffinokat izomerizáló eljárások is
továbbfejlődtek.
A zeolitok szóba jöhetnek az izoolefinek és a
metanol reakciójának katalizátoraként is, mivel róluk a szénlerakódás
regenerálással eltávolítható, és így újra használhatók, míg a jelenleg
használatos ioncserélő műgyanták nem. Az így kapott éterek fontos
oktánszámjavító komponensek. A másik fontos oktánszámnövelő eljárás,
amelyikben zeolitok is szóba jöhetnek, az i-bután alkilezése
olefinekkel. Néhány szabadalom H-zeolitok alkalmazásáról szól. A
zeolitok előnyösen helyettesíthetnék a jelenleg használatos, de nagyon
korrozív tömény kénsavat, illetve HF-ot.
Jelenleg az olajfeldolgozó ipar olyan új
eljárásokat és katalizátorokat igényel, amelyekkel a különböző
viszkózus nehézolaj frakciók az eddigieknél hatékonyabban
feldolgozhatók. Ebből a szempontból ígéretes lehet új, mezopórusos
szilikátok felfedezése, mivel ezek pórusmérete a jelenleg használatos
Y zeolitokénál nagyobb, így nagyobb méretű szénhidrogén molekulák
tudnak adszorbeálódni és krakkolódni.
A rézioncserélt zeolitok, különösen a ZSM-5
változat nemcsak a mozgó, de az álló szennyező források esetén is
ígéretes katalizátorok a nitrogén-oxidok eltávolítására.
Hazai zeolitok és zeolitkutatás
Magyarországon a Zempléni-hegységben és Tokaj környékén vannak
bányászható mennyiségű és minőségű, mordenitet és klinoptilolitot
tartalmazó ásványok. Korábban az Országos Érc- és Ásványbányák
Hegyaljai Üzeme Mádon, ma pedig a belőle kivált gazdasági társulás
foglalkozik a természetes zeolit bányászatával és értékesítésével
(Hannus – Kiricsi, 2003).
Hazánk vegyipari fejlettségének és kapacitásának
megfelelően nálunk nincs katalizátorgyártó ipar. Saját technológiához
a MOL RT. százhalombattai telepén gyártanak zeolit katalizátort.
Adszorpciós célokra korábban a Reanal Finomvegyszergyár Molfilit
néven, a Budapesti Vegyiművek pedig Klinosorb márkanéven forgalmazott
zeolitokat.
Ma világszerte, így Magyarországon is az egyre
szigorodó környezetvédelmi előírásoknak megfelelően a foszfátmentes
mosóporok adalékanyagaként felhasznált zeolitok jelentik a legnagyobb
mennyiséget. 1995-ben kezdte meg a termelést Ajkán egy 20 ezer t/év
kapacitású, NaA zeolitot gyártó üzem, amely a szintézisben az Al
nyersanyagaként a timföldgyár hulladék aluminátlúgját használja, míg a
Si-nyersanyag vízüveg.
Magyarország nemcsak természetes zeolit
előfordulásokban gazdag, hanem a zeolit szintézise és alkalmazása
területén is bővelkedik itthon és külföldön élő szakemberekben. Rabó
Gyula Amerikában él, a Magyar Tudományos Akadémia külső tagja, a UOP
(Universal Oil Products) volt kutatási igazgatója, akinek neve
összeforrott a zeolitok katalitikus alkalmazásával, elsősorban a
petrolkémiai iparban. Csicsery Zsigmond, aki a zeolit katalizátorok
alakszelektív hatásának első rendszerezője, a Chevron Co. volt
munkatársa. B. Nagy János belgiumi professzor a zeolitok szintézisének
és NMR spektroszkópiás tanulmányozásának nemzetközi hírű kutatója. A
hazai zeolitkutatás úttörői Beyer Hermann, Fejes Pál és Kalló Dénes
voltak. Tanítványaik közül többen napjainkban is a zeolitkutatás
területén tevékenykednek
Hazánkban több egyetemi és akadémiai kutatóhelyen
foglalkoznak a zeolitok eredetének, tulajdonságainak vizsgálatával és
hasznosításuk lehetőségeivel. Ezek a szakemberek iparban dolgozó
kollégáikkal együtt 1991-ben hozták létre és azóta működtetik szakmai
szervezetüket, a Magyar Zeolit Társaságot. A társaság a FEZA
(Federation of European Zeolite Association) tagjaként Kiricsi Imre
vezetésével szervezte 1999-ben Egerben az első, hagyományteremtő FEZA
konferenciát. 2011-ben a spanyolországi Valenciában tartották az
ötödiket.
A zeolitok a túlzott algásodást okozó foszfátok helyettesítőiként
mosóporadalékként, a savas esőt okozó és más káros gázok megkötésével
adszorpciós tulajdonságaik révén, és nem utolsósorban katalizátorként
a környezetvédelem fontos anyagai. A zeolitok egyre nagyobb szerepet
kapnak az intermedierek és a finomvegyszer-végtermékek előállításában
is. A molekulaszűrők új generációjának kifejlesztésével, a zeolitok
tulajdonságainak pontosabb kialakításával minden alkalmazásra
előállítható a testre szabott katalizátor.
Amikor a különböző környezetszennyezésekért a kémiát okolják, és nem a
tudatlan vagy felelőtlen emberi tevékenységet, akkor fontos rámutatni,
különösen most, a Kémia Nemzetközi Éve kapcsán, hogy egészséges
környezet nem lesz a kémia és a kémikusok hozzájárulása nélkül.
A cikk a TÁMOP 4.2.1/B-09/1/KONV-2010-0005 azonosító számú,
Kutatóegyetemi Kiválósági Központ létrehozása a Szegedi
Tudományegyetemen című pályázat anyagi támogatásával készült.
Kulcsszavak: természetes zeolit, szintézis, adszorpció, ioncsere,
katalízis, környezetvédelem
IRODALOM
B. Nagy János – Bodart, P. – Hannus I. –
Kiricsi I. (1998): Synthesis, Characterization and Use of Zeolitic
Microporous Materials. DecaGen Ltd., Szeged, Hungary
Dyer, Alan (1988): An Introduction to
Zeolite Molecular Sieves. John Wiley, New York
Hannus István – Kiricsi Imre (2003):
Zeolitok a XXI. század küszöbén. Természet Világa. 134, 452.
Hlavay József – Pataki K. – Kovács Gy. I.
(szerk.) (1987): Hazai természetes zeolitok kutatása és felhasználása.
(2.) MTA VEAB, Veszprém
Venuto, Paul B. – Habib, E. Thomas (1979):
Fluid Catalytic Cracking with Zeolite Catalysts. Marcel Dekker, New
York
|